Vật lí Nhiệt
I. MÔ HÌNH ĐỘNG HỌC PHÂN TỬ VỀ CẤU TẠO CHẤT.
Những nội dung cơ bản của mô hình động học phân tử về cấu tạo chất:
- Các chất được cấu tạo từ các hạt riêng biệt là phân tử.
- Các phân tử chuyển động không ngừng. Nhiệt độ của vật càng cao thì các phân tử chuyển động càng nhanh.
- Giữa các phân tử có lực đẩy và lực hút, gọi chung là lực liên kết phân tử: Khi khoảng cách giữa các phân tử nhỏ thì lực đẩy mạnh hơn lực hút, khi khoảng cách giữa các phân tử lớn thì lực hút mạnh hơn lực đẩy. Khi khoảng cách giữa các phân tử rất lớn thì lực tương tác không đáng kể.
Dùng mô hình này có thể giải thích được cấu trúc các chất rắn, lỏng, khí và sự chuyển thể.
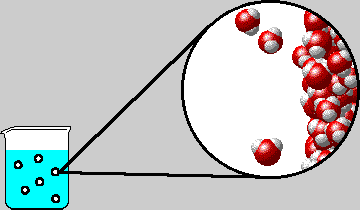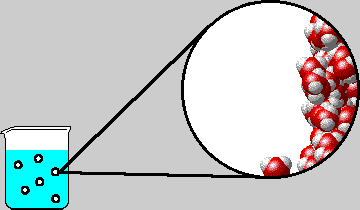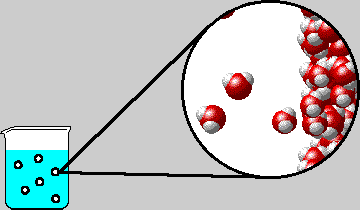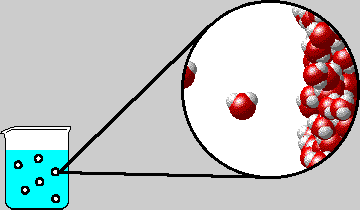
II. CẤU TRÚC CỦA CHẤT RẮN, CHẤT LỎNG VÀ CHẤT KHÍ.
Để nêu được sơ lược về cấu trúc của hầu hết chất rắn, lỏng, khí, ta cần nắm những đặc điểm sau:
- Khi khoảng cách giữa các phân tử lớn thì lực liên kết giữa chúng sẽ yếu.
- Các phân tử sắp xếp có trật tự thì lực liên kết giữa chúng mạnh.
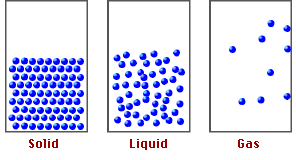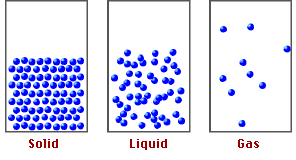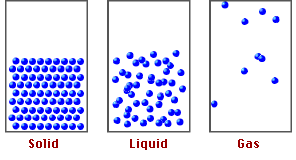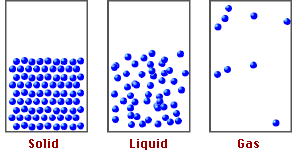
* Ở thể rắn: Khoảng cách giữa các phân rất nhỏ, lực tương tác giữa các phân tử rất mạnh nên giữ được các phân tử ở các vị trí cân bằng xác định, làm cho chúng chỉ có thể dao động xung quanh các vị trí này. Các vật rắn có thể tích và hình dạng riêng xác định.
| Chất rắn vô định hình | Chất rắn Kết tinh | |
|---|---|---|
|
- Chất rắn vô định hình là các chất không có cấu trúc tinh thể và do đó không có dạng hình học xác định.
- Các chất rắn vô định hình có tính đẵng hướng và không có nhiệt độ nóng chảy xác định. Khi bị nung nóng, chúng mềm dần và chuyển sang thể lỏng. |
- Các chất rắn kết tinh cho dù được cấu tạo từ cùng một loại hạt, nhưng nếu cấu trúc tinh thể không giống nhau thì những tính chất vật lí của chúng cũng rất khác nhau. - Mỗi chất rắn kết tinh ứng với mỗi cấu trúc tinh thể có một nhiệt độ nóng chảy xác định không dổi ở mỗi áp suất cho trước. - Chất rắn kết tinh có thể là chất đơn tinh thể hoặc chất đa tinh thể. |
|
| Chất đơn tinh thể có tính dị hướng. | Chất đa tinh thể có tính đẵng hướng. | |
* Ở thể khí: Khoảng cách giữa các phân rất xa, lực tương tác giữa các phân tử rất yếu nên các phân tử chuyển động hoàn toàn hỗn loạn. Chất khí không có hình dạng và thể tích riêng.
* Ở thể lỏng: Khoảng cách giữa các phân lớn hơn so với chất rắn nhưng nhỏ hơn so với chất khí, lực tương tác giữa các phân tử lớn hơn ở thể khí nhưng nhỏ hơn ở thể rắn, nên các phân tử dao động xung quanh vị trí cân bằng có thể di chuyển được. Chất lỏng có thể tích riêng xác định nhưng không có hình dạng riêng mà có hình dạng của phần bình chứa nó.
III. SỰ CHUYỂN THỂ.
1. Sự chuyển thể.
Đa số các chất ở thể rắn, khi nóng lên có thể chuyển sang thể lỏng, rồi từ thể lỏng sang thể khí. Ngược lại, đa số chất khí, khi lạnh đi sẽ chuyển sang thể lỏng, rồi từ thể lỏng sang thể rắn.
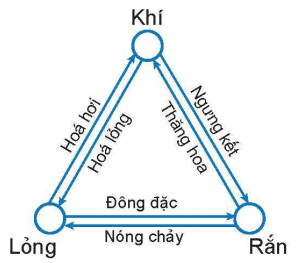
2. Dùng mô hình động học phân tử giải thích sự chuyển thể.
Để giải thích được sơ lược về sự chuyển thể, ta cần nắm những đặc điểm sau: Trong khi chuyển động hổn loạn, các phân tử có thể va chạm vào nhau và truyền năng lượng cho nhau. Càng nhận nhiều năng lượng thì các phân tử chuyển động hỗn loạn càng nhanh, khoảng cách trung bình giữa chúng càng tăng, lực liên kết giữa chúng càng giảm.
a. Giải thích sự hóa hơi: là quá trình chuyển từ thể lỏng sang thể hơi. Gồm hai hình thức là sự bay hời và sự sôi.
- Sự bay hơi: là sự hóa hơi xảy ra ở mặt thoáng của chất lỏng.
Nguyên nhân: do các phân tử chuyển động hỗn loạn và chạm vào nhau, truyền năng lượng cho nhau, nên có một số phân tử ở gần mặt thoáng của chất lỏng có động năng đủ lớn để thắng lực liên kết của các phân tử chất lỏng khác, thoát được ra khỏi mặt thoáng của chất lỏngtrở thành các phân tử thể hơi. .
- Sự sôi: là sự hóa hơi xảy ra đồng thời ở bên trong và mặt thoáng của chất lỏng.
Nguyên nhân: Khi sôi các bọt chứa không khí và hơi nước nổi lên trong lòng nước ngày càng nhiều, càng nổi lên trên thể tích các bọt khí càng tăng, tới mặt thoáng thì vỡ, không khí và hời nước thóa ra ngoài khí quyển thành thể hơi.
b. Giải thích sự nóng chảy của chất rắn kết tinh: là quá trình chuyển từ thể rắn sang thể lỏng.
Nguyên nhân: khi nhân nhiệt độ, các ion nút mạng dao động nhiệt càng mạnh, đến mức phá vỡ cấu trúc mạng tinh thể, từ đó không còn hình dạng xác định và chuyển sang thể lỏng.
I. KHÁI NIỆM NỘI NĂNG.
1. Nội năng của một vật.
- Nội năng của vật là tổng động năng và thế năng của các phân tử cấu tạo nên vật. Kí hiệu nội năng là U, đơn vị là J.
- Nội năng của một vật phụ thuộc vào nhiệt độ và thể tích của vật: U = f(T, V)
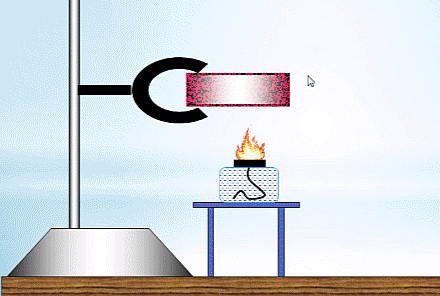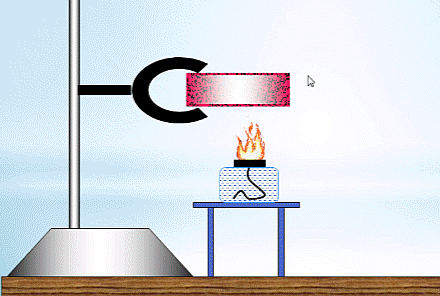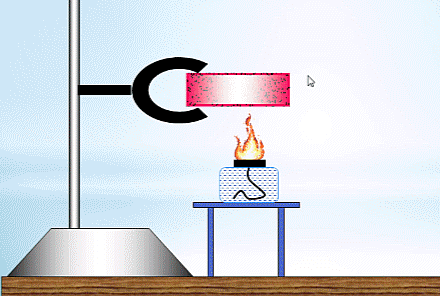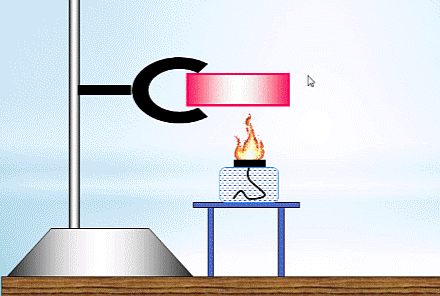
2. Thí nghiệm về mối liên hệ nội năng của vật với năng lượng của các phân tử cấu tạo nên vật.

- Chuẩn bị:
+ Ống nghiệm có nút đậy.
+ Đèn cồn.
+ Giá đở.
- Tiến hành: Bố trí thí nghiệm như hình vẽ. Đun nóng ống nghiệm cho đến khi nút bấc bật ra.
- Nhận xét:
+ Khi đun nóng, các phân tử nhận nhiệt lượng, chuyển hóa thành động năng phân tử.
+ Khi động năng phân tử tăng dẫn đến nội năng khối khí tăng lên. Đến lúc động năng phân tử đủ lớn thì nút ống nghiệm bật ra.
I. ĐỊNH LUẬT I CỦA NHIỆT ĐỘNG LỰC HỌC.
1. Cách làm thay đổi nội năng.
Có hai cách làm biến đổi nội năng là thực hiện công và truyền nhiệt.
- Thực hiện công: Khi thực hiện công lên hệ hoặc cho hệ thực hiện công thì có thể làm thay đổi nội năng của hệ. Trong quá trình thực hiện công thì có sự biến đổi qua lại giữa nội năng và dạng năng lượng khác.

- Truyền nhiệt: Quá trình làm thay đổi nội năng không có sự thực hiện công gọi là quá trình truyền nhiệt. Trong quá trình truyền nhiệt không có sự chuyển hoá năng lượng từ dạng này sang dạng khác mà chỉ có sự truyền nội năng từ vật này sang vật khác.
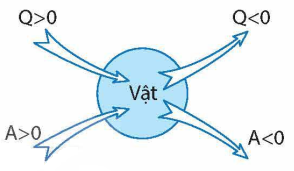
2. Định luật I của nhiệt động lực học. Độ biến thiên nọi năng của một vật bằng tổng công và nhiệt lượng mà vật nhận được.
ΔU= A + Q
- Qui ước dấu:
| ΔU> 0: nội năng tăng | ΔU< 0: nội năng giảm. |
| A> 0: hệ nhận công | A< 0: hệ thực hiện (sinh) công |
| Q> 0: hệ nhận nhiệt | Q< 0: hệ truyền (tỏa) nhiệt |
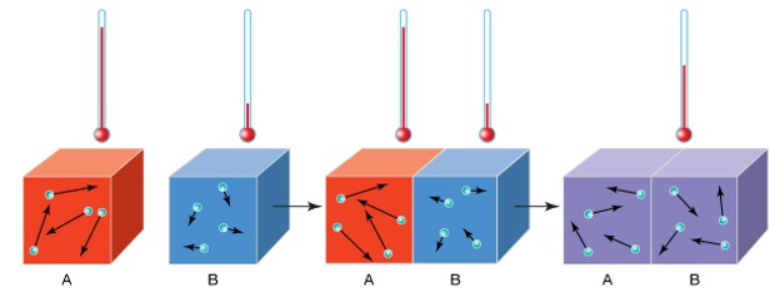
I. KHÁI NIỆM NHIỆT ĐỘ.
Nhiệt độ cho biết trạng thái cân bằng nhiệt của các vật tiếp xúc nhau và chiều truyền nhiệt năng:
- Khi hai vật có nhiệt độ chênh lệch tiếp xúc nhau thì nhiệt năng truyền từ vật có nhiệt độ cao hơn sang vật có nhiệt độ thấp hơn.
- Khi hai vật tiếp xúc nhau có nhiệt độ bằng nhau thì không có sự truyền nhiệt năng giữa chúng. Hai vật ở trạng thái cân bằng nhiệt.
II. THANG NHIỆT ĐỘ - NHIỆT KẾ.
1. Các thang nhiệt độ.
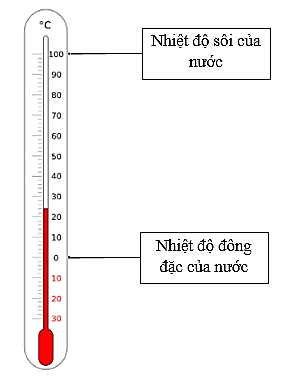
a. Thang nhiệt độ Celsius:
- Thang Celsius là thang đo nhiệt độ có một mốc là nhiệt độ nóng chảy của nước đá tinh khiết (quy ước là 00C) và mốc còn lại là nhiệt độ sôi của nước tinh khiết (quy ước là 1000C). Khoảng giữa hai mốc nhiệt độ này được chia thành 100 khoảng bằng nhau, mỗi khoảng là 10.
- Nhiệt độ trong thang Celsius thường được kí hiệu bằng chữ t, đơn vị là độ C (0C).
- Các nhiệt độ cao hơn 00C có giá trị dương, thấp hơn 00C có giá trị âm.
- Thang nhiệt độ chúng ta vẫn dùng hằng ngày là thang Celsius.
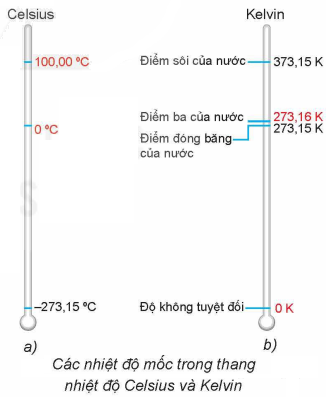
a. Thang nhiệt độ Kelvin:
- Thang nhiệt độ Kelvin, còn được gọi là thang đo nhiệt độ nhiệt động lực học, là thang đo nhiệt độ sử dụng mốc gồm hai nhiệt độ cố định:
- Nhiệt độ thấp nhất mà các vật có thể có, được gọi là độ không tuyệt đối, được định nghĩa là 0K. Không có vật ở bất kì trạng thái nào có thể có nhiệt độ thấp hơn nhiệt độ này.
- Nhiệt độ mà nước tinh khiết có thể tồn tại đồng thời ở cả ba thể rắn, lỏng và hơi, trong trạng thái cân bằng nhiệt ở áp suất tiêu chuẩn (được định nghĩa là 273,16K, tương đương với 0,010C), được gọi là nhiệt độ điểm ba của nước.
\(T(K)=t(^0C)+273,15\)
a. Thang nhiệt độ Fahrenheit:
- Trong thang này, nhiệt độ nước đá tan là 320F, của nước đang sôi là 2120F
\(t(^0F)=1,8t(^0C)+32\)
2. Nhiệt kế.
- Nhiệt kế là thiết bị dùng để đo nhiệt độ. Nhiệt kế được chế tạo dựa trên một số tính chất vật lí phụ thuộc vào nhiệt độ của các chất, các vật liệu, các linh kiện điện và điện tử,….
- Tính chất vật lí được sử dụng nhiều ở đây là sự nở vì nhiệt.
\(l=l_0(1+\alpha \Delta t)\)
+ Sự phụ thuộc của điện trở vào nhiệt độ.
\(R=R_0(1+\alpha \Delta t)\)
+ Sự phụ thuộc của hiệu điện thế cặp nhiệt điện vào nhiệt độ.
\(\xi=\alpha_T (t_{nóng}-t_{nguội})\)
+ Sự phụ thuộc của bước sóng điện từ vào nhiệt độ.
\(\lambda_{max}T=2900\mu mK\)
I. KHÁI NIỆM NHIỆT DUNG RIÊNG.
1. Hệ thức tính nhiệt lượng trong quá trình truyền nhiệt để làm thay đổi nhiệt độ của vật.

- Thực nghiệm chứng tỏ rằng: Nhiệt lượng Q cần truyền cho vật để làm cho nó nóng lên tỉ lệ thuận với khối lượng m của vật và độ tăng nhiệt Δt độ của vật.
\(\frac{Q}{m\Delta T}= hằng số\)
với mỗi chất, hằng số trên có giá trị riêng và được gọi là nhiệt dung riêng c. Do đó, ta có biểu thức nhiệt dung riêng:
\(c= \frac{Q}{m\Delta T}\)
trong đó:
+ Q là nhiệt lượng truyền cho vật (J)
+ m là khối lượng của vật (kg)
+ ΔT là biến thiên nhiệt độ (K)
+ c là nhiệt dung riêng (\(\frac{J}{kg.K}\))
- Từ biểu thức trên, ta thu được biểu thức tính nhiệt lượng trong quá trình truyền nhiệt để làm thay đổi nhiệt độ của vật là:
\(Q= mc\Delta T\)
2. Định nghĩa nhiệt dung riêng.
- Nhiệt dung riêng của một chất là nhiệt lượng cần truyền cho 1kg chất đó để làm cho nhiệt độ của nó tăng thêm 10C.
- Nhiệt dung riêng là một thông tin quan trọng thường được dùng trong khi thiết kế các hệ thống làm mát, sưởi ấm,...
| Chất | Nhiệt dung riêng (J/(kg.K) |
|---|---|
| Nước | 4200 |
| Nước đá | 2100 |
| Không khí | 1000 |
| Thủy tinh | 840 |
| Đất | 800 |
| Sắt | 440 |
| Đồng | 380 |
| Thủy ngân | 140 |
| Chì | 130 |
II. THỰC HÀNH ĐO NHIỆT DUNG RIÊNG CỦA NƯỚC.
1. Mục đích thí nghiệm.
Xác định nhiệt dung riêng của nước.
2. Dụng cụ thí nghiệm.
• Biến thế nguồn (1).
• Bộ đo công suất nguồn điện (oát kế) có tích hợp chức năng đo thời gian (2).
• Nhiệt kế điện từ hoặc cảm biến điện từ hoặc cảm biến nhiệt độ có thang đo từ -200C đến 1100C và độ phân giải ±,10C (3).
• Nhiệt lượng kế bằng nhựa có vỏ xốp, kèm điện trở nhiệt (gắn ở trong bình) (4).
• Cân điện tử (5) (hoặc bình đong).
• Các dây nối.

3. Thiết kế phương án thí nghiệm.
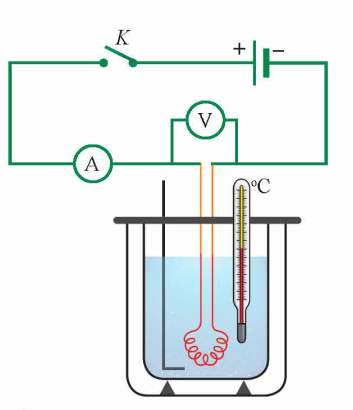
4. Tiến hành thí nghiệm.
- Đổ một lượng nước vào bình nhiệt lượng kế, sao cho toàn bộ điện trở nhiệt chìm trong nước, xác định khối lượng nước này.
- Cắm đầu đo của nhiệt kế vào nhiệt kế vào nhiệt lượng kế vào nhiệt lượng kế
- Nối oát kế với nhiệt lượng kế và nguồn điện.
- Bật nguồn điện.
- Khuấy liên tục để nước nóng đều. Cứ sau mỗi khoảng thời gian 1 phút đọc công suất dòng điện từ oát kế, nhiệt độ từ nhiệt kế rồi điền kết quả vào vở theo mẫu tương tự Bảng 4.2.
- Tắt nguồn điện.
Bảng 4.2. Khối lượng nước m=0,15g.
| Nhiệt độ t(0C) | Thời gian τ(s) | Công suất P (W) |
|---|---|---|
| 25,2 | ||
| 25,4 | ||
| 27 | ||
| 28,7 | ||
| 31,2 | ||
| 32,3 | ||
| 33,8 |
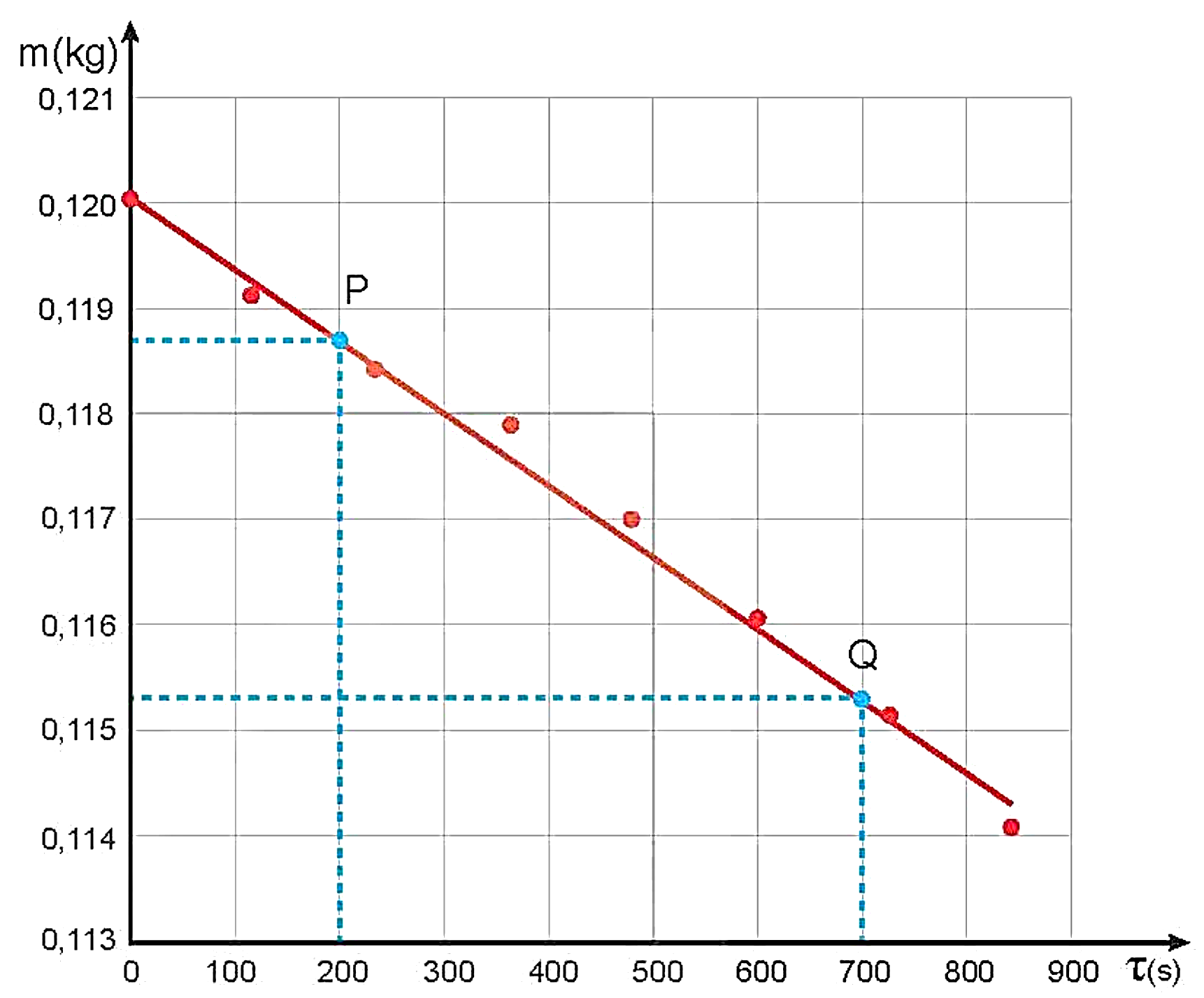
5. Kết quả thí nghiệm.
Vẽ đồ thị nhiệt độ của nước theo thời gian.
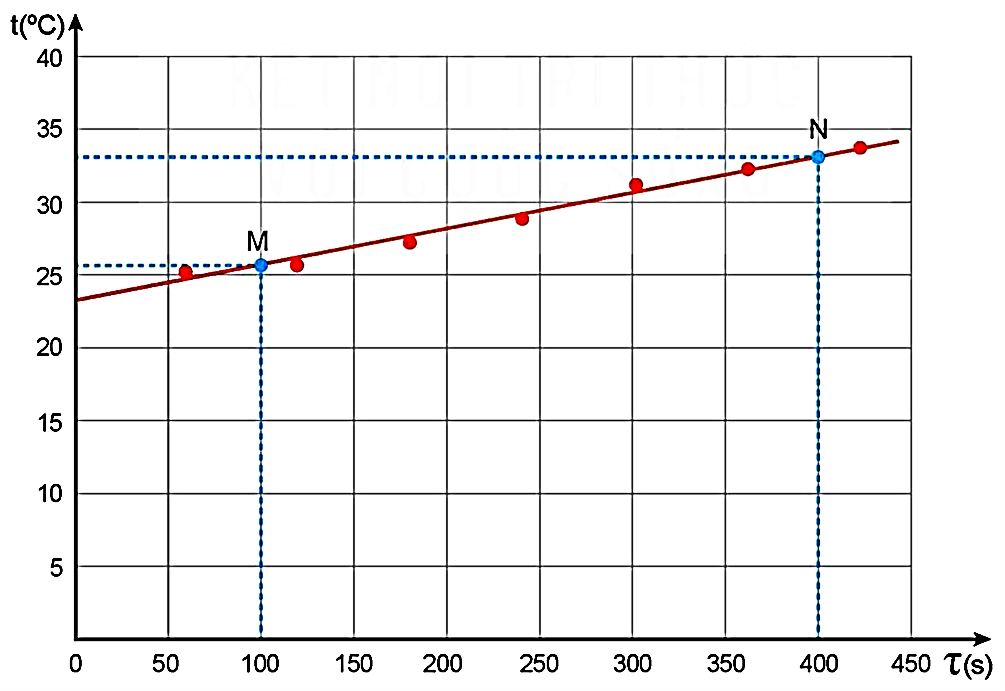
I. KHÁI NIỆM NHIỆT NÓNG CHẢY RIÊNG.
1. Hệ thức tính nhiệt lượng trong quá trình truyền nhiệt để làm vật nóng chảy hoàn toàn.

- Thực nghiệm chứng tỏ rằng: Nhiệt lượng Q cần truyền cho vật khi vật bắt đầu nóng chảy tới khi vật nóng chảy hoàn toàn phụ thuộc vào khối lượng m của vật và tính chất của vật.
\(\frac{Q}{m}= hằng số\)
với mỗi chất, hằng số trên có giá trị riêng và được gọi là nhiệt nóng chảy riêng λ. Do đó, ta có biểu thức nhiệt nóng chảy riêng:
\(\lambda= \frac{Q}{m}\)
trong đó:
+ Q là nhiệt lượng truyền cho vật (J)
+ m là khối lượng của vật (kg)
+ λ là nhiệt nóng chảy riêng (\(\frac{J}{kg}\))
- Từ biểu thức trên, ta thu được biểu thức tính nhiệt lượng trong quá trình truyền nhiệt để làm vật nóng chảy hoàn toàn là:
\(Q= \lambda m\)
2. Định nghĩa nhiệt nóng chảy riêng.
- Nhiệt nóng chảy riêng của một chất là nhiệt lượng cần để làm cho một đơn vị khối lượng chất đó nóng chảy hoàn toàn ở nhiệt độ nóng chảy mà không làm thay đổi nhiệt độ.
- Nhiệt nóng chảy riêng và nhiệt độ nóng chảy là những thông tin giúp xác định được năng lượng cần cung cấp cho lò nung, thời gian nung, thời điểm đổ kim loại nóng chảy vào khuôn, thời điểm lấy sản phẩm ra khỏi khuôn. Các đại lượng này cũng cần thiết cho việc lựa chọn kim loại để chế tạo hợp kim, hay tách kim loại ra từ quặng hỗn hợp.
| Chất | Nhiệt độ nóng chảy t(0C) | Nhiệt nóng chảy riêng (J/kg) |
|---|---|---|
| Nước đá | 0 | 3,34.105 |
| Sắt | 1535 | 2,77.105 |
| Đồng | 1084 | 1,8.105 |
| Chì | 327 | 0,25.105 |
II. THỰC HÀNH ĐO NHIỆT NÓNG CHẢY RIÊNG CỦA NƯỚC ĐÁ.
1. Mục đích thí nghiệm.
Xác định nhiệt nóng chảy riêng của nước đá.
2. Dụng cụ thí nghiệm.
• Biến thế nguồn (1).
• Bộ đo công suất nguồn điện (oát kế) có tích hợp chức năng đo thời gian (2).
• Nhiệt kế điện từ hoặc cảm biến điện từ hoặc cảm biến nhiệt độ có thang đo từ -200C đến 1100C và độ phân giải ±,10C (3).
• Nhiệt lượng kế bằng nhựa có vỏ xốp, kèm điện trở nhiệt (gắn ở trong bình) (4).
• Cân điện tử (5) (hoặc bình đong).
• Các dây nối.

3. Thiết kế phương án thí nghiệm.
4. Tiến hành thí nghiệm.
- Cho các viên nước đá hoặc một ít nước lạnh vào bình nhiệt lượng kế, sao cho toàn bộ dây điên trở chìm trong nước đá Xác định khối lượng hỗn hợp nước đá trong bình.
- Cắm đầu đo cûa nhiệt kế vào bình nhiệt lượng kế.
- Nối oát kế với nhiệt lượng kế và nguồn điện.
- Bật nguồn điện.
- Khuấy liên tục nước đá, cứ sau mỗi khoảng thời gian 2 phút lại đọc số đo thời gian trên oát kế và nhiệt độ trên nhiệt kế rồi ghi kết quả vào vở theo mẫu tương tự Bảng 5.2.
- Tắt nguồn điện.
Bảng 5.2. Khối lượng nước m=0,25g.
| Thời gian τ(s) | Nhiệt độ t(0C) | Công suất P (W) |
|---|---|---|
| 0 | ||
| 120 | ||
| 240 | ||
| 360 | ||
| 480 | ||
| 600 | ||
| 720 | ||
| 840 | ||
| 960 |
5. Kết quả thí nghiệm.
Vẽ đồ thị nhiệt độ của nước theo thời gian.
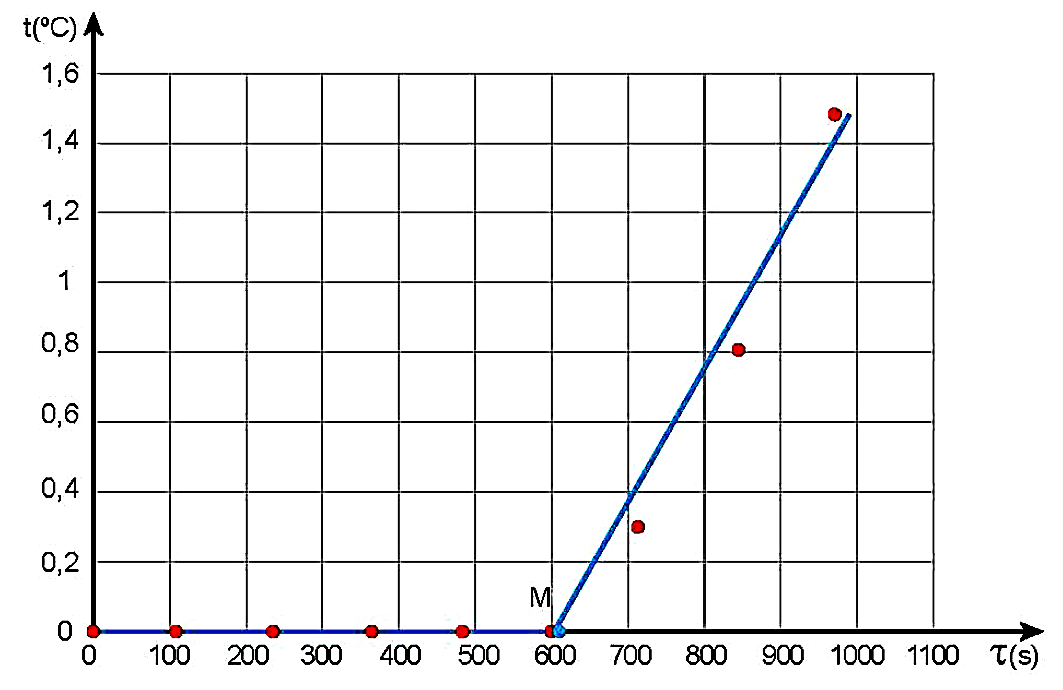
I. KHÁI NIỆM NHIỆT HÓA HƠI RIÊNG.
1. Hệ thức tính nhiệt lượng trong quá trình truyền nhiệt khi một lượng chất lỏng hóa hơi ở nhiệt độ không đổi.

- Thực nghiệm chứng tỏ rằng: Nhiệt lượng Q cần cung cấp cho một lượng chất lỏng hóa hơi ở nhiệt độ không đổi phụ thuộc vào khối lượng m của vật và bản chất của chất lỏng.
\(\frac{Q}{m}= hằng số\)
với mỗi chất, hằng số trên có giá trị riêng và được gọi là nhiệt hóa hơi riêng L. Do đó, ta có biểu thức nhiệt hóa hơi riêng:
\(L= \frac{Q}{m}\)
trong đó:
+ Q là nhiệt lượng truyền cho chất lỏng (J)
+ m là khối lượng của chất lỏng (kg)
+ L là nhiệt hóa hơi riêng (\(\frac{J}{kg}\))
- Từ biểu thức trên, ta thu được biểu thức tính nhiệt lượng cần cung cấp cho một lượng chất lỏng hóa hơi hoàn toàn ở nhiệt độ không đổi là:
\(Q= Lm\)
2. Định nghĩa nhiệt hóa hơi riêng.
- Nhiệt hoá hơi riêng của một chất lỏng là nhiệt lượng cần để làm cho một kilogam chất lỏng đó hoá hơi hoàn toàn ở nhiệt độ xác định.
- Nhiệt hoá hơi riêng là thông tin cần thiết trong việc thiết kế, chế tạo sản phẩm có sự dụng hiện tượng hoá hơi nhằm tiết kiệm năng lượng, bảo vệ môi trường
| Chất | Nhiệt độ sôi t(0C) | Nhiệt hóa hơi riêng (J/kg) |
|---|---|---|
| Nước | 100 | 2,26.106 |
| Rượu | 78 | 8,57.105 |
| Thủy ngân | 357 | 2,85.105 |
| Ether | 34,5 | 4.105 |
II. THỰC HÀNH ĐO NHIỆT HÓA HƠI RIÊNG CỦA NƯỚC.
1. Mục đích thí nghiệm.
Xác định nhiệt hoá hơi riêng của nước ở nhiệt độ sôi (1000C)
2. Dụng cụ thí nghiệm.
• Biến thế nguồn (1).
• Bộ đo công suất nguồn điện (oát kế) có tích hợp chức năng đo thời gian (2).
• Nhiệt kế điện từ hoặc cảm biến điện từ hoặc cảm biến nhiệt độ có thang đo từ -200C đến 1100C và độ phân giải ±,10C (3).
• Nhiệt lượng kế bằng nhựa có vỏ xốp, kèm điện trở nhiệt (gắn ở trong bình) (4).
• Cân điện tử (5) (hoặc bình đong).
• Các dây nối.
• Một lượng nước nóng.

3. Thiết kế phương án thí nghiệm.
- Để xác định nhiệt hoá hơi riêng của nước cần xác định nhiệt lượng cần cung cấp cho nước hoá hơi và khối lượng của nước.
- Nhiệt lượng làm cho nước trong bình nhiệt lượng kế hoá hơi lấy từ nguồn điện.
- Đảm bảo an toàn trong khi tiến hành thí nghiệm như: kiểm tra các thiết bị trước khi sử dụng tuân thủ các quy tắc an toàn khi làm việc với nguồn nhiệt và thiết bị điện, sử dụng các dụng cụ bảo hộ, tránh tiếp xúc trực tiếp với nguồn nhiệt và giữ khoảng cách an toàn.
4. Tiến hành thí nghiệm.
- Đặt nhiệt lượng kế lên cân. Đổ nước nóng vào nhiệt lượng kế. Xác định khối lượng nước trong bình.
- Tháo nắp bình ra khỏi nhiệt lượng kế.
- Nối oát kế với điện trở và nguồn điện.
- Đặt dây điện trở vào nhiệt lượng kế sao cho toàn bộ dây chìm trong nước.
- Bật nguồn điện.
- Đun sôi nước trong bình nhiệt lượng kế. Sau mỗi khoảng thời gian 2 phút, đọc số đo công suất trên oát kế, khối lượng nước trong bình nhiệt lượng kế trên cân. Ghi kết quả vào bảng theo mẫu.
- Tắt nguồn điện.
5. Kết quả thí nghiệm.
Bảng 6.2.
| Thời gian τ(s) | Khối lượng (kg) | Công suất P (W) |
|---|---|---|
| 0 | ||
| 120 | ||
| 240 | ||
| 360 | ||
| 480 | ||
| 600 | ||
| 720 | ||
| 840 | ||
| 960 |
Vẽ đồ thị nhiệt độ của nước theo thời gian.
T(K)= t(0C) +273;
t(0F) = 32 + 1,8.t(0C)
Câu 1. Mô hình động học phân tử về cấu tạo chất.
- Các chất được cấu tạo từ các hạt riêng biệt là phân tử.
- Các phân tử chuyển động không ngừng. Nhiệt độ của vật càng cao thì các phân tử chuyển động càng nhanh.
- Giữa các phân tử có lực đẩy và lực hút, gọi chung là lực liên kết phân tử: Khi khoảng cách giữa các phân tử nhỏ thì lực đẩy mạnh hơn lực hút, khi khoảng cách giữa các phân tử lớn thì lực hút mạnh hơn lực đẩy. Khi khoảng cách giữa các phân tử rất lớn thì lực tương tác không đáng kể.
Câu 2. Nội năng- Các cách làm thay đổi nội năng.
- Nội năng của vật là tổng động năng và thế năng của các phân tử cấu tạo nên vật. Nội năng của một vật phụ thuộc vào nhiệt độ và thể tích của vật: U = f(T, V)
- Các cách làm thay đổi nội năng.
+ Thực hiện công: Khi thực hiện công lên hệ hoặc cho hệ thức hiện công thì có thể làm thay đổi nội năng của hệ. Trong quá trình thực hiện công thì có sự biến đổi qua lại giữa nội năng và dạng năng lượng khác.
+ Truyền nhiệt: Quá trình làm thay đổi nội năng không có sự thực hiện công gọi là quá trình truyền nhiệt. Trong quá trình truyền nhiệt không có sự chuyển hoá năng lượng từ dạng này sang dạng khác mà chỉ có sự truyền nội năng từ vật này sang vật khác.
* Nhiệt lượng mà vật nhận được hay mất đi (khi thể tích của vật không đổi):
Q = mcΔt.
* Trong hệ cô lập thì tổng nhiệt lượng tỏa ra bằng tổng nhiệt lượng thu vào:
|Qtỏa| = Qthu hay Qtỏa + Qthu = 0
Câu 3. Nguyên lí I nhiệt động lực học: Độ biến thiên nội năng của một vật bằng tổng công và nhiệt lượng mà vật nhận được.
ΔU= A + Q
- Qui ước dấu:
| ΔU> 0: nội năng tăng | ΔU< 0: nội năng giảm. |
| A> 0: hệ nhận công | A< 0: hệ thực hiện (sinh) công |
| Q> 0: hệ nhận nhiệt | Q< 0: hệ truyền (tỏa) nhiệt |

Câu 4. Quá trình thuận nghịch và không thuận nghịch.
- Quá trình thuận nghịch: là quá trình vật tự trở về trạng thái ban đầu mà không cần đến sự can thiệp của vật khác.
- Quá trình không thuận nghịch: là quá trình chỉ có thể xảy ra theo một chiều xác định, không thể tự xảy ra theo chiều ngược lại. Muốn xảy ra theo chiều ngược lại phải cần đến sự can thiệp của vật khác.
Câu 5. Nguyên lí II nhiệt động lực học.
- Cách phát biểu của Clau-di-út: Nhiệt không thể tự truyền từ một vật sang một vật nóng hơn.
- Cách phát biểu của Các-nô: Động cơ nhiệt không thể chuyển hoá tất cả nhiệt lượng nhận được thành công cơ học.
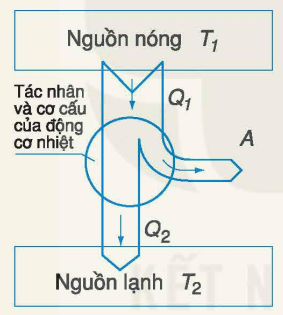
- Nguyên tắc cấu tạo và hoạt động của động cơ nhiệt: Mỗi động cơ nhiệt đều phải có ba bộ phận cơ bản là:
+ Nguồn nóng để cung cấp nhiệt lượng (Q1).
+ Bộ phận phát động gồm vật trung gian nhận nhiệt sinh công (A) gọi là tác nhân và các thiết bị phát động.
+ Nguồn lạnh để thu nhiệt lượng do tác nhân toả ra (Q2).
- Hiệu suất của động cơ nhiệt:
\(H=\frac{|A|}{Q_1}=\frac{Q_1-Q_2}{Q_1} < 1\)
Câu 6. Cấu trúc của chất rắn, lỏng, khí.
- Ở thể khí, lực tương tác giữa các phân tử rất yếu nên các phân tử chuyển động hoàn toàn hỗn loạn. Chất khí không có hình dạng và thể tích riêng.
- Ở thể rắn, lực tương tác giữa các phân tử rất mạnh nên giữ được các phân tử ở các vị trí cân bằng xác định, làm cho chúng chỉ có thể dao động xung quanh các vị trí này. Các vật rắn có thể tích và hình dạng riêng xác định.
- Ở thể lỏng, lực tương tác giữa các phân tử lớn hơn ở thể khí nhưng nhỏ hơn ở thể rắn, nên các phân tử dao đông xung quanh vị trí cân bằng có thể di chuyển được. Chất lỏng có thể tích riêng xác định nhưng không có hình dạng riêng mà có hình dạng của phần bình chứa nó.
Câu 7. Sự chuyển thể. Đa số các chất ở thể rắn, khi nóng lên có thể chuyển sang thể lỏng, rồi từ thể lỏng sang thể khí. Ngược lại, đa số chất khí, khi lạnh đi sẽ chuyển sang thể lỏng, rồi từ thể lỏng sang thể rắn.

Câu 8. Sự nóng chảy: là quá trình chuyển từ thể rắn sang thể lỏng.
- Mỗi chất rắn kết tinh có một nhiệt độ nóng chảy xác định ở mỗi áp suất cho trước.
- Các chất rắn vô định hình không có nhiệt độ nóng chảy xác định.
- Đa số các chất rắn, thể tích của chúng sẽ tăng khi nóng chảy và giảm khi đông đặc.
- Nhiệt độ nóng chảy của chất rắn thay đổi phụ thuộc vào áp suất bên ngoài.
* Nhiệt nóng chảy: Nhiệt lượng Q cần cung cấp cho chất rắn trong quá trình nóng chảy gọi là nhiệt nóng chảy.
\(Q=\lambda.m\)
với λ là nhiệt nóng chảy riêng phụ thuộc vào bản chất của chất rắn nóng chảy, có đơn vị là J/kg.
Câu 9. Sự hóa hơi: gồm sự bay hơi và sự sôi.
a. Sự bay hơi: là quá trình chuyển từ thể lỏng sang thể khí ở bề mặt chất lỏng. Quá trình ngược lại từ thể khí sang thể lỏng gọi là sự ngưng tụ. Sự bay hơi xảy ra ở nhiệt độ bất kì và luôn kèm theo sự ngưng tụ.
- Khi tốc độ bay hơp lớn hơn tốc độ ngưng tụ, áp suất hơi tăng dần và hơi trên bề mặt chất lỏng là hơi khô.
- Khi tốc độ bay hơi bằng tốc độ ngưng tụ, hơi ở phía trên mặt chất lỏng là hơi bảo hoà có áp suất đạt giá trị cực đại gọi là áp suất hơi bảo hoà.
- Áp suất hơi bảo hoà không phụ thuộc thể tích và không tuân theo định luật Bôi-lơ – Ma-ri-ôt, nó chỉ phụ thuộc vào bản chất và nhiệt độ của chất lỏng.
b. Sự sôi: là sự chuyển từ thể lỏng sang thể khí xảy ra ở cả bên trong và trên bề mặt chất lỏng gọi là sự sôi.
* Nhiệt hoá hơi: Nhiệt lượng Q cần cung cấp cho khối chất lỏng trong khi sôi gọi là nhiệt hoá hơi của khối chất lỏng ở nhiệt độ sôi.
\(Q=L.m\)
với L là nhiệt hoá hơi riêng phụ thuộc vào bản chất của chất lỏng bay hơi, có đơn vị là J/kg.
